Biogipuzkoa Osasun Ikerketarako Institutuko Zelula Amak eta Zahartzea taldeko ikertzaileek plataforma baten propietateak garatu eta probatu dituzte, laborategian melanoma eta haren metastasia zehaztasun handiagoz ikertzeko. Paula Vázquez-Aristizabal, Inazio Arriola-Alvarez, Sonia Alonso-Martin eta Ander Izeta lankideek, Bionanoplasmonics Lab-eko (CIC biomaGUNE) ikertzaileekin eta Herbehereetako Mimetas BV enpresarekin batera egin dute lan hau, eta emaitzak ACS Applied Bio Materials nazioarteko aldizkari zientifikoan argitaratu dira.
Melanoma (larruazaleko tumorea) minbizi oldarkorrenetako bat da, barreiatzeko gaitasun handia duelako, bai odoletik, bai linfatik. Proiekzio batzuen arabera, 2040. urterako % 50eko igoera aurreikusten da, eta, beraz, terapia eraginkorragoak garatzeko beharra kritikoa da, batez ere gaur egun erabiltzen diren medikamentuekiko (Vemurafenib eta Encorafenib) erresistentziak agertzen direnean. Egungo azterketa-ereduak ez direnez nahikoa gaixotasun horren konplexutasuna jasotzeko, ezinbestekoa da plataforma esperimental fidagarriagoak diseinatzea, gizakiengan erantzun terapeutikoa arrakastaz aurreikustea ahalbidetuko dutenak.
Erronka horri aurre egiteko, lan berri honetan proposatu zen mikrofluido-sistema aurreratuetan integratzea zelulaz kanpoko matrize deszelularizatuak (dECM). Kolageno-hidrogel konbentzionalek ez bezala, dECMk funtsezko seinale biologikoak eta propietate biomimetikoak babesten ditu zelulek beren portaera organismo erreal batean erreplika dezaten. Helburu nagusia, beraz, melanoma baskularizatuaren eredu bat garatzea izan zen. Eredu horrek zehatz-mehatz birsortzen ditu odol-konpartimentuak eta linfatikoak, eta sendotutako eta errendimendu handiko (high-throughput) plataforma gisa finkatzen da sendagaiak testatzeko eta tumore-progresioa aztertzeko. Horrela, eta Paula Vázquez-Aristizabalek eta kolaboratzaileek 2024an garatutako ereduan oinarrituta, errendimendu handiko melanoma mikrofluidikoaren eredu berria garatu zen.
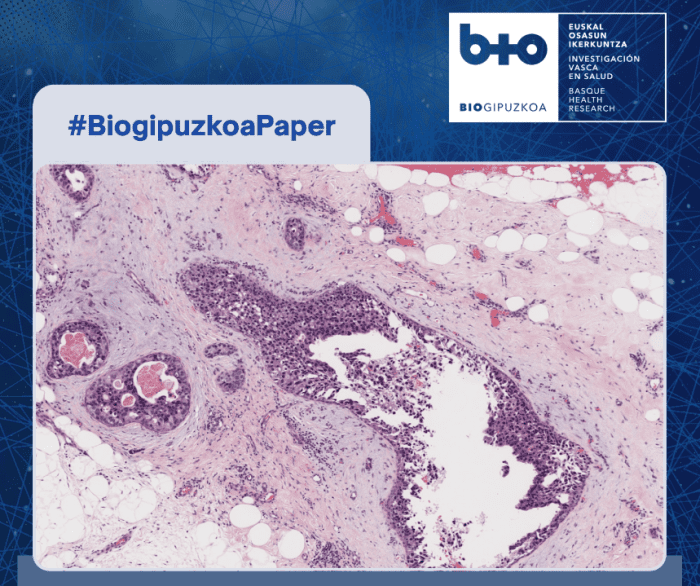
Ikerketaren emaitzak izan ziren, alde batetik, OrganoPlate Graft plataforma erabiliz, trikultura-sistema bat birsortzea lortu zen. Sistema horretan, melanoma-esferoideek zuzenean elkarreragiten dute txerri-dermiseko dECM batekin eta egitura baskular (odolekoa eta linfatikoa) funtzionalekin (Mimetismoa jatorrizko mikroingurunearekin). Bestetik, melanomaren barreiatze metastasikoaren hasierako etapak simulatu zituen ereduak, tumore-zelulek ondoko ehun eta hodietan duten inbasioa monitorizatu ahal izan baitzuen (hasierako metastasiaren laburpena). Azkenik, toxikotasunaren eta tumorearen aurkako erantzunaren saiakuntzetan, ereduak sentikortasun konparagarria erakutsi zuen in vivo azterketetan lortutako emaitzekin. Zehazki, sistemak zehaztasunez bereizi zuen eraginkortasun terapeutikoa BRAF genearen inhibitzaileen artean, eta Encorafenib farmakoak Vemurafenib farmakoaren aurrean duen nagusitasuna erakutsi zuen, egungo ebidentzia klinikoarekin lerrokatuz (baliozkotze farmakologikoa).
Beraz, eredu honek melanomaren ikerketarako ingurune paregabea eskaintzen du eta modelizazioan hobekuntza nabarmena eskatzen du. Horrela, ehunetik eratorritako dECMak erabiltzeak I motako kolagenozko hidrogel konbentzionalak baino ingurune molekular aberatsagoa eta fisiologikoki handiagoa eskaintzen du, tumore-nitxoa (biomimetismoa) modu fidelagoan birsortzeko aukera emanez. Era berean, arrakastaz baliozkotu da esferoide heterotipikoak sare baskular bikoitzekin (odolekoa eta linfatikoa) organ-on-a-chip gailu batean integratzea, melanomaren egitura-konplexutasuna in vivo (zelula-konplexutasuna) imitatzen duen arkitektura lortuz. Aldi berean, frogatuta geratu da eredua baliagarria dela azterketa terapeutikorako kontzeptu-proba gisa, eta tumore-portaera eta sendagaiei ingurune kontrolatu baina konplexu batean ematen zaien erantzuna ebaluatzeko duen gaitasuna azpimarratu da (egokia da baheketa-plataforma gisa). Eredua erreproduzigarritasun eta estandarizazio handiagatik nabarmentzen da, pazienteen zuzeneko laginen berezko aldakortasuna gaindituz. Hori tresna ezin hobea da industria-aplikazioetarako eta eskala handiko farmakoen baheketarako (erreproduzigarritasuna eta estandarizazioa). Azkenik, etorkizunean pazienteetatik eratorritako organoideak eta giza dECM integratzeak eredu horiek pertsonalizatzea ahalbidetuko luke. Horrek sistema iragarpen klinikorako tresna bihurtuko luke, estrategia terapeutiko indibidualak optimizatzeko, “saiakuntza eta errore” ikuspegia minimizatuz eta pazientearen bizi-kalitatea hobetuz (medikuntza pertsonalizatua izateko potentziala).
Horregatik guztiagatik, ondoriozta daiteke lan honen inpaktua hiru zutabetan oinarritzen dela. Lehenik eta behin, tratamendu azkarragoak eta seguruagoak lortzeko aukera; izan ere, tumorearen ingurune erreala birsortzean (odol-hodiak eta linfa-hodiak barne), farmakoak proba daitezke giza gorputza simulatzen duen eszenatoki batean, eta horrek pazientearentzako terapia berrien etorrera bizkortzen du, saiakuntza klinikoetan itxarote-denbora murriztuz. Bigarrenik, medikuntza pertsonalizatua ahalbidetzea; izan ere, eredu horri esker, hobeto uler daiteke melanoma nola hedatzen den, hau da, tumore horren metastasia nola hedatzen den. Horrek esan nahi du, etorkizunean, paziente bati tratamendu erasokor bat aplikatu aurretik, bere eredu pertsonalizatuan testatu ahal izango dela, funtzionatuko ote duen aurreikusteko, eraginkortasunik gabeko farmakoen alferrikako albo-ondorioak saihestuz. Azkenik, animalien esperimentazioa murriztea ahalbidetuko da; izan ere, azaleko dECMak erabiltzean, animalia-ereduak, zeintzuen erantzunak ez dira beti gizakienak bezalakoak izaten, baino aukera etiko eta zehatzagoak sortzen dira, eta horien.
Eredu hori jauzi kualitatibo bat bada ere, hasierako garapen-etapa batean dago. Hurrengo urrats logikoa funtsezko osagaiak integratzea izango litzateke, hala nola immunitate-sistema; horri esker, fideltasun handiagoa lortuko litzateke in vitro melanoma birsortzean.
Ikertzaileen hitzetan, “oso harro gaude in vitro eredu hau aurkezteaz, etorkizun handiko ikerketa-aldi bizi bat amaitzen duen lorpenarekin. Asko gustatzen zaigu aurrerapen horrekin gaixotasunen modelizazioaren arloan laguntzea, laborategiko zientzia pazientearen benetako beharretara hurbiltzen duen tresna bat eskainiz. Gure helburu nagusia sistema hori ingurune klinikoan finkatu arte eboluzionatzea da, medikuntza pertsonalizaturako nahiz melanomaren edo beste gaixotasun batzuen tratamendua eraldatuko duten terapia berriak identifikatzeko funtsezko pieza bihurtuz“.