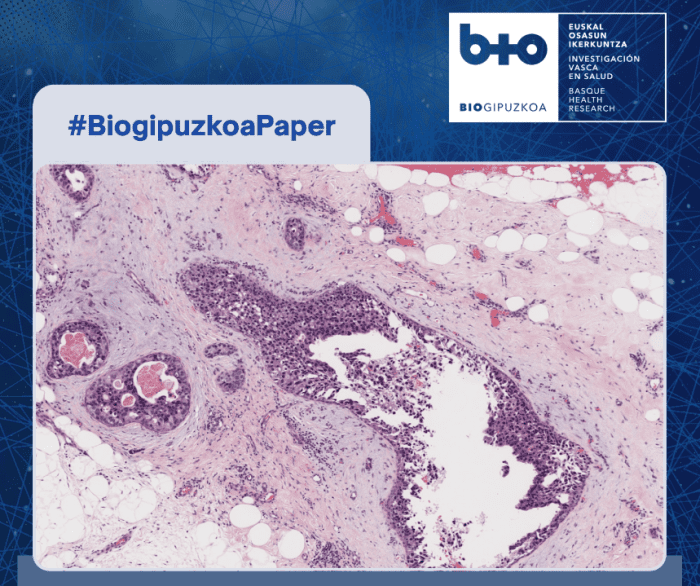
Investigadoras e investigadores del grupo Células Madre y Envejecimiento del Instituto de Investigación Sanitaria Biogipuzkoa, han desarrollado y probado las propiedades de una plataforma para investigar con mayor precisión el melanoma y su metástasis en laboratorio. Las y los compañeros Paula Vázquez-Aristizabal, Inazio Arriola-Alvarez, Sonia Alonso-Martin y Ander Izeta, junto a investigadores de Bionanoplasmonics Lab (CIC biomaGUNE) y la empresa holandesa Mimetas BV, han realizado este trabajo, cuyos resultados se han publicado en la revista científica internacional ACS Applied Bio Materials.
El melanoma (tumor en la piel) destaca como uno de los cánceres más agresivos debido a su excepcional capacidad de diseminación, tanto por vía sanguínea como linfática. Hay proyecciones que estiman un incremento del 50% en su incidencia para el año 2040, por lo que la necesidad de desarrollar terapias más eficaces es crítica, especialmente ante la aparición de resistencias a los fármacos que se utilizan actualmente como son el Vemurafenib y el Encorafenib. Dado que los modelos de estudio actuales resultan insuficientes para capturar la complejidad de esta enfermedad, existe una necesidad imperiosa de diseñar plataformas experimentales más fidedignas que permitan predecir con éxito la respuesta terapéutica en humanos.
Para abordar este desafío, en este nuevo trabajo se propuso la integración de matrices extracelulares descelularizadas (dECM) en sistemas de microfluídica avanzados. A diferencia de los hidrogeles de colágeno convencionales, la dECM preserva las señales biológicas y propiedades biomiméticas esenciales para que las células repliquen su comportamiento en un organismo real. El objetivo primordial, por lo tanto, fue desarrollar un modelo de melanoma vascularizado que recrea con precisión tanto los compartimentos sanguíneos como los linfáticos, consolidándose como una plataforma robusta y de alto rendimiento (high-throughput) para el testado de fármacos y el estudio de la progresión tumoral. De este modo, y basándose en el modelo desarrollado previamente por Paula Vázquez-Aristizabal y colaboradores en 2024, se desarrolló el nuevo modelo de melanoma microfluídico de alto rendimiento.
Como resultados de la investigación, por un lado, mediante el uso de la plataforma OrganoPlate Graft, se logró recrear un sistema de tricultivo donde esferoides de melanoma interaccionan directamente con una dECM de dermis porcina y estructuras vasculares (sanguínea y linfática) funcionales (Mimetismo con el microambiente nativo). Por otro, el modelo simuló las etapas iniciales de la diseminación metastásica del melanoma, al poder monitorizar la invasión de las células tumorales al tejido y vasos adyacentes (Recapitulación de la metástasis inicial). Por último, en los ensayos de toxicidad y respuesta antitumoral, el modelo exhibió una sensibilidad comparable a los resultados obtenidos en estudios in vivo. Específicamente, el sistema discriminó con precisión la eficacia terapéutica entre los inhibidores del gen BRAF, mostrando una superioridad del fármaco Encorafenib frente al Vemurafenib, alineándose con la evidencia clínica actual (Validación Farmacológica).
Por lo tanto, este modelo ofrece un entorno único para la investigación del melanoma y postula una mejora sustancial en su modelización. Así, se ha conocido que el uso de dECMs derivadas de tejido ofrece un entorno molecularmente más rico y fisiológicamente superior a los hidrogeles convencionales de colágeno tipo I, permitiendo una recreación más fiel del nicho tumoral (Biomimetismo). Tambien se ha validado con éxito la integración de esferoides heterotípicos con redes vasculares dobles (sanguínea y linfática) dentro de un dispositivo organ-on-a-chip, logrando una arquitectura que imita la complejidad estructural del melanoma in vivo (Complejidad celular). Al mismo tiempo, se ha demostrado la utilidad del modelo como prueba de concepto para el testado terapéutico, subrayando su capacidad para evaluar el comportamiento tumoral y la respuesta a fármacos en un entorno controlado pero complejo (Apto como plataforma de cribado). El modelo destaca por su alta reproducibilidad y estandarización, superando la variabilidad inherente de las muestras directas de pacientes. Esto lo posiciona como una herramienta óptima para aplicaciones industriales y cribado de fármacos a gran escala (Reproducibilidad y estandarización). Por último, la futura integración de organoides derivados de pacientes y dECM humana permitiría personalizar estos modelos. Esto transformaría el sistema en una herramienta de predicción clínica para optimizar estrategias terapéuticas individuales, minimizando el enfoque de «ensayo y error» y mejorando la calidad de vida del paciente (Potencial como medicina personalizada).
Por todo ello, se puede concluir que el impacto de este trabajo se sustenta en tres pilares. En primer lugar, la posibilidad de lograr tratamientos más rápidos y seguros, ya que al recrear el entorno real del tumor (incluyendo vasos sanguíneos y linfáticos), se pueden probar fármacos en un escenario que simula al cuerpo humano, lo que acelera la llegada de nuevas terapias al paciente, reduciendo el tiempo de espera en ensayos clínicos. En segundo lugar, posibilitar una medicina personalizada, ya que este modelo permite entender mejor cómo se propaga el melanoma, es decir, la metástasis de este tumor, lo que a futuro podría implicar que, antes de aplicar un tratamiento agresivo a un paciente, se pueda testar en su propio modelo personalizado para predecir si funcionará, evitando efectos secundarios innecesarios de fármacos ineficaces. Por último, permitir una reducción de la experimentación animal, ya que al usar dECMs de piel, se crean alternativas más éticas y, a menudo, más precisas que los modelos animales, cuyas respuestas no siempre son iguales a las de humano.
Si bien este modelo representa un salto cualitativo, se encuentra en una etapa inicial de desarrollo. El siguiente paso lógico sería la integración de componentes clave como el sistema inmunitario, lo que permitirá alcanzar una mayor fidelidad en la recreación del melanoma in vitro.
En palabras de las y los investigadores “estamos muy orgullosas y orgullosos de poder presentar este modelo in vitro, un logro que culmina un intenso periodo de investigación con un resultado prometedor. Nos entusiasma contribuir con este avance al campo de la modelización de enfermedades, aportando una herramienta que acerca la ciencia de laboratorio a las necesidades reales del paciente. Nuestra mayor aspiración es que este sistema evolucione hasta consolidarse en el entorno clínico, convirtiéndose en una pieza clave tanto para la medicina personalizada como para la identificación de nuevas terapias que transformen el tratamiento del melanoma u otras enfermedades”.